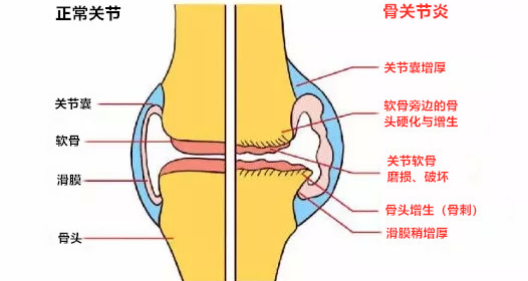
骨关节炎(OA)是由多种因素引起的关节软骨纤维化、皲裂、溃疡、脱失而导致的以关节疼痛为主要症状,严重影响患者生活质量的退行性疾病。OA分为原发性和继发性。原发性OA多发生于中老年人群,无明确的全身或局部诱因,与遗传和体质因素有一定的关系。而继发性OA可发生于青壮年,继发于创伤、炎症、关节不稳定、积累性劳损或先天性疾病等。
骨关节炎发病的机制主要有:①基因:OA 为基因相关性疾病,是多基因共同作用的结果。②细胞因子 ( cytokines,CK ):关节组织的损伤是由细胞因子、生长因子 ( growth factor )、蛋白酶类 ( protease ) 和炎症因子( inflammatory factors ) 共同介导的。③基质金属蛋白酶 ( matrixmatalloproteinase,MMPs ):研究表明,OA关节软骨中的 MMPs 合成增加, MMPs 特异性抑制物 ( tissue inhibitor of metalloproteinases,TIMPs)合成减少,导致软骨细胞外基质的合成与降解失衡。④免疫因素:近年来的研究表明,免疫因素在OA的发生发展中起重要作用。⑤软骨细胞凋亡:软骨细胞是成熟软骨组织内惟一的细胞类型,它在软骨损伤以及重塑过程中起到维持内环境稳定的作用。